Une bonne utilisation des antibiotiques permettrait d'améliorer la durée de vie des patients atteints de mucoviscidose
Par la rédaction de bioMérieux | Temps de lecture : 3 min
DATE DE PUBLICATION : 2 AOÛT 2023
Trente-cinq à quarante ans, c’est l’espérance de vie moyenne des patients atteints de mucoviscidose aux États-Unis et au Royaume-Uni. « Ce qui représente une amélioration considérable sachant qu’elle était de 10 ans, il y a quelques dizaines d’années seulement, explique le docteur Andrea Hahn, spécialiste des maladies infectieuses pédiatriques au Children's National Health System de Washington. Une des clés pour aider les patients à vivre aussi longtemps, c’est l’utilisation raisonnée d’antibiotiques ».
Les antibiotiques « sont une arme à double tranchant » ajoute le Dr Hahn : « Bien qu'ils soient nécessaires pour éradiquer les infections pulmonaires, leur usage répété peut provoquer une antibiorésistance, ce qui complique le traitement des infections futures. L'usage d'antibiotiques peut également tuer les bactéries non pathogènes présentes dans les poumons. Cela diminue la diversité de la communauté microbienne pulmonaire, facteur associé à la progression de la maladie. »
Mais, on ne sait pas exactement comment l'antibiorésistance influe sur la relation entre la diversité des bactéries pulmonaires et la fonction pulmonaire des patients atteints de mucoviscidose. Une équipe du Children's National a publié une étude visant à répondre à cette interrogation (l’article est en accès libre (en anglais) : Antibiotic multidrug resistance in the cystic fibrosis airway microbiome is associated with decreased diversity). Elle suggère, dans un communiqué de presse que « la présence de bactéries multirésistantes dans les voies respiratoires des patients atteints de mucoviscidose est associée à une diminution de la diversité microbienne et de la fonction pulmonaire. »
Antibiorésistance chez les patients atteints de mucoviscidose
Les symptômes caractéristiques de la mucoviscidose se manifestent par une congestion pulmonaire chronique accompagnée d'une toux persistante, d'infections pulmonaires fréquentes, d'une respiration haletante et d'un essoufflement. La mucoviscidose est une maladie génétique progressive dans laquelle les patients héritent de deux copies défectueuses du gène du régulateur de la conductance transmembranaire de la mucoviscidose (cystic fibrosis transmembrane conductance regulator, CFTR, en anglais), chacune provenant d'un des parents. Les gènes mutés entraînent un dysfonctionnement de la protéine CFTR, ce qui rend le mucus normal - dans différents organes notamment les poumons - épais et collant.
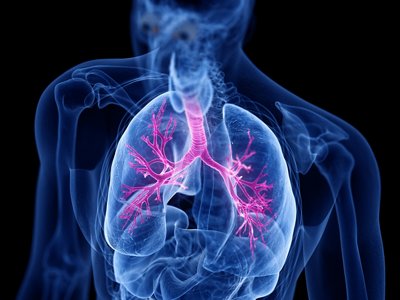
Le mucus obstrue les voies respiratoires du patient et emprisonne des germes qui sont à l'origine d'infections et d'autres complications, notamment le développement de colonies bactériennes appelées « films biologiques » dans les poumons. Les films biologiques bactériens sont des communautés bactériennes structurées qui produisent une matrice polymère protégeant la colonie. Le comportement des bactéries des films biologiques est différent de celui des bactéries isolées qui comportent plusieurs membres, développant des morphologies et des fonctionnalités différentes.
Point essentiel : les bactéries des films biologiques sont plus résistantes aux antibiotiques que les bactéries isolées. C'est la raison pour laquelle les stratégies de lutte contre les infections liées à la mucoviscidose doivent « combattre la croissance des films biologiques, éviter l'apparition d'une résistance mutationnelle, favoriser le développement de nouveaux antibiotiques contre les souches multirésistantes et mettre en œuvre des mesures strictes de lutte contre l'infection. »
Dans l'étude du Children's National, les chercheurs ont analysé de manière détaillée les sécrétions respiratoires de 6 patients atteints de mucoviscidose pendant 18 mois. Ils ont découvert une grande variété d'espèces bactériennes, dont le Staphylococcus aureus résistant à la méthicilline (SARM). Ces patients, ainsi que les autres sujets atteints d'une infection antibiorésistante, présentaient « une diversité microbienne significativement plus faible dans leurs échantillons et une forme plus agressive. »
« L'usage prolongé d'antibiotiques a probablement contribué à l'antibiorésistance et à la diminution de la diversité microbienne chez ces patients », selon le Docteur Hahn. « Cependant, a-t-elle poursuivi, la réduction de l'usage des antibiotiques chez les patients atteints de mucoviscidose n'est pas la solution ». En effet, sans antibiotiques, de nombreux patients atteints de mucoviscidose ne survivraient pas aux exacerbations pulmonaires récurrentes qui sont monnaie courante.
Des outils de diagnostic pour lutter contre l'antibiorésistance et orienter le traitement des patients atteints de mucoviscidose
Il est essentiel de limiter la surconsommation et le mauvais usage des antibiotiques dans la lutte contre l'antibiorésistance. Cela nécessite l’utilisation d’outils de diagnostic rapide pour permettre les décisions de prescription précises et rapides. Si l'usage des antibiotiques peut se révéler nécessaire, il est important qu’il soit raisonné. « Il est impossible d'arrêter les antibiotiques » déclare le Docteur Hahn « mais il est possible d'apprendre à mieux les utiliser. » Pour cela, elle préconise la mise en place d'un laboratoire de microbiologie plus proactif afin de surveiller de près les types d'infections liées à la mucoviscidose et d'identifier les antibiotiques auxquels chaque infection est la plus sensible.
Dans l'étude du Children's National, les chercheurs ont analysé chaque échantillon de deux manières différentes : la culture en laboratoire standard et les tests moléculaires. « Les cultures en laboratoire sont conçues pour cultiver certains types de bactéries qui sont connues pour être problématiques mais elles ne révèlent pas tout » explique le Docteur Hahn. « Le séquençage génétique de ces échantillons nous permet de tout voir. » Les tests moléculaires rapides effectués sur des échantillons prélevés sur des patients atteints de mucoviscidose peuvent sauver des vies, d’autant plus que, chez de nombreux patients, l'infection est provoquée par plusieurs espèces de microbes.
Un article de la revue MDPI, Antibiotic Resistance in Patients with Cystic Fibrosis: Past, Present, and Future, présente les outils de pointe et les données de la séquence du génome entier créées par les plateformes de séquençage de nouvelle génération (next-generation sequencing, NGS) et la façon dont ils peuvent se révéler utiles. Les outils NGS se sont révélés plus rapides et plus efficaces que les techniques moléculaires traditionnelles. Les plateformes NGS offrent également la possibilité d'une analyse horizontale du résistome, dont la « détection des gènes de résistance acquise et des mutations chromosomiques pertinentes ». Bien que la recherche et la technologie modernes aient permis d'améliorer le traitement des patients atteints de mucoviscidose, des recherches supplémentaires sont nécessaires pour continuer à progresser.
« Les recherches devraient porter en priorité sur la mise en place de meilleurs outils de diagnostic, comme le séquençage métagénomique et la transcriptomique de nouvelle génération qui peuvent détecter directement l'antibiorésistance dans les communautés microbiennes colonisant les voies respiratoires des patients atteints de mucoviscidose » expliquent les auteurs de l'étude de MDPI. « La présence de l'antibiorésistance reste un problème de santé essentiel pour les patients atteints de mucoviscidose. La gestion et le suivi de l'usage des antibiotiques sont obligatoires et plus pertinents que jamais. »
Les avis exprimés dans cet article ne sont pas nécessairement ceux de bioMérieux.
VOUS SEREZ PEUT-ÊTRE INTÉRESSÉS PAR CES ARTICLES...
SHARE THIS:
- AMR AMS
< SWIPE FOR MORE ARTICLES >
-2?qlt=85&ts=1690552882061&dpr=off)
